
中大新聞網訊(通訊員趙現廷)10月1日,中山大學腫瘤防治中心徐瑞華教授團隊領銜的一項1b期臨床研究(NCT05890742)發表于國際頂級期刊Cancer Cell。研究采用前瞻性隨機對照設計,系統評估了信達生物伊匹木單抗N01(IBI310)聯合信迪利單抗對比PD-1單藥,在局部進展期微衛星高度不穩定/錯配修復缺陷(MSI-H/dMMR)結腸癌新輔助治療中的療效與安全性。首次以高水平的循證證據驗證中國雙免方案可顯著提高病理完全緩解率(pCR)達78.4%,在中位隨訪21.4個月內無患者復發,安全耐受,為優化該類患者的新輔助治療模式提供了有力支持。

研究以封面文章發表于Cancer Cell
封面展示的是黃河與洮河的交界處,它位于甘肅省臨夏回族自治州永靖縣境內,兩河于此相擁——渾濁湍急的洮河攜著黃土高原的赭黃,與湛清緩流的黃河水相遇,形成一道“半江碧水半江渾”的天然奇觀。正如我們Neoshot IB臨床研究中CTLA4抗體IBI310(洮河)如烈馬奔騰而下,注入PD-1抗體信迪利單抗(黃河)的懷抱,二者碰撞交融,涇渭分明卻又最終合一,最終將黃河渲染成大地的血脈。猶如歷史長河在此刻定格——既是自然的磅礴詩篇,也是民族生生不息的隱喻。
結直腸癌是全球第三大常見惡性腫瘤,也是癌癥相關死亡的第二原因。約有15%的結直腸癌患者存在微衛星高度不穩定/錯配修復缺陷(MSI-H/dMMR),該類腫瘤因其高突變負荷,產生大量新抗原,使得腫瘤微環境對免疫治療更為敏感。既往針對局部晚期(Ⅱ-Ⅲ期)MSI-H/dMMR患者的治療,盡管手術是核心治療手段,但高危患者(如T4或N2)術后復發風險較高,而傳統新輔助化療對dMMR腫瘤療效有限。近年來,免疫檢查點抑制劑(ICIs)在轉移性MSI-H/dMMR結直腸癌中展現出顯著療效,推動了其在局限性腫瘤新輔助治療中的探索。然而,ICIs在新輔助治療中的價值,尤其是雙免疫聯合方案能否較單藥帶來更好的獲益,目前相關數據較為有限。
本研究是一項隨機對照、開放標簽、多中心1b期臨床試驗(NCT05890742),研究共納入101名局部晚期可切除MSI-H/dMMR結腸癌患者,隨機分配雙免疫方案組(n=52),接受伊匹木單抗N01注射液(IBI310)+信迪利單抗治療,共2個治療周期;或單藥組(n=49),接受信迪利單抗單藥治療。新輔助治療后進行手術評估。主要終點為改良意向治療人群(mITT)(接受至少一次新輔助治療且完成手術)的pCR率,次要終點包括無事件生存期(EFS)、總生存期(OS)、R0切除率和安全性。

研究方案設計
病理完全緩解率達78.4%,中國雙免方案創造新紀錄
mITT中,雙免疫方案組病理完全緩解率(pCR)率高達78.4%,顯著高于單藥組的46.7%,組間差異為28.3%(95% CI: 10.8-45.7, p=0.0015)。意向治療人群(ITT)和符合方案人群(PP)亦得出一致結果,分別為76.9%和80%,均支持聯合用藥顯著提高pCR。
與既往研究中ICIs單藥新輔助治療的pCR率59%–65%及雙免疫聯合治療的pCR率60%–68%相比,均實現大幅提升,刷新歷史記錄,為結腸癌新輔助免疫治療領域帶來全新突破。
此外,雙免疫方案組主要病理緩解率(MPR)率也高達94.1%(殘留活腫瘤細胞RVT ≤10%),優于單藥組73.3%,與NICHE-2研究(MPR 95%)和NICHE-3研究(MPR 92%)結果相當,這一結果足以反映出中國雙免方案優于PD-1單藥治療的臨床獲益。
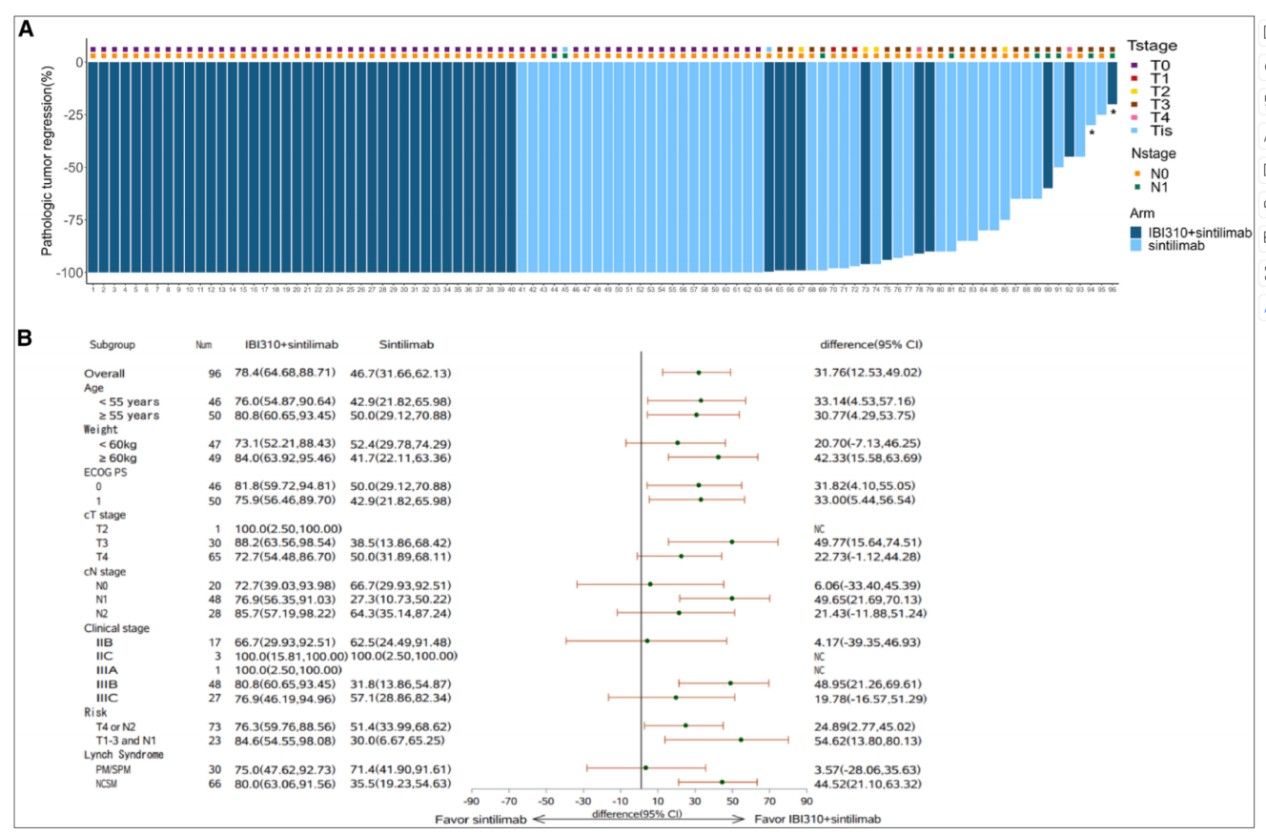
主要終點病理完全緩解率
在分層亞組分析中,研究進一步揭示了不同遺傳背景及臨床分型對療效的影響。非林奇綜合征相關突變患者中,雙免疫方案組的pCR率高達80.0%,遠高于單藥組的35.5%,組間差異36.7%(95% CI: 16.7-56.7)。而攜帶林奇綜合征致病性/或疑似致病性突變患者,兩組pCR率均超過70%,差異不顯著。
所有患者實現R0切除,21.4個月中位隨訪期內無復發
接受標準治療(包括手術和輔助治療)的局部晚期dMMR結腸癌患者實現R0切除挑戰大且復發率風險較高。在本研究中,盡管76.2%的患者屬于高危人群,但所有患者均成功實現R0切除,術后中位隨訪時間為21.4個月(范圍:1.5-24.6),在隨訪期間未見疾病復發,意味著雙免疫新輔助治療可能大幅降低遠期復發風險。目前,EFS與OS數據仍在持續隨訪中,其長期生存獲益值得進一步期待。
安全可控,中國雙免方案無新增風險
安全性方面,治療相關不良事件(TRAEs)發生率在雙免疫方案組為71.2%,單藥組為49.0%;≥3級TRAEs發生率分別為3.8%和10.2%。多數TRAEs為1-2級,提示兩種治療方案均具有良好耐受性,且聯合用藥未顯著增加嚴重不良事件風險。
免疫相關不良事件(irAEs)發生率在雙免疫方案組為48.1%,單藥組為38.8%。≥3級irAEs發生率分別為3.8%(包括免疫性心肌炎和腸炎)和8.2%(包括免疫性心肌炎、皮疹、甲狀腺功能減退和丙氨酸氨基轉移酶升高)。手術期并發癥及死亡率在兩組中均無統計學差異,未出現新的安全信號。
此外,一項隨機對照、多中心Ⅲ期臨床試驗(NeoShot-III研究,NCT05890742)正在進行中,將進一步驗證雙免疫治療方案與術后輔助化療在MSI-H/dMMR結腸癌患者中的療效與安全性,為其成為MSI-H/dMMR結腸癌新輔助治療方案提供更充分的循證證據支持。
作為隨機對照用于MSI-H/dMMR結腸癌新輔助治療的臨床研究,試驗采用的伊匹木單抗N01(IBI310)與信迪利單抗均為我國自主研發的原研藥物。本研究成功發表于國際頂刊Cancer Cell,是中國腫瘤臨床研究創新邁向世界前沿的有力印證。“中國雙免方案”凝聚中國智慧,立足中國需求,更展現了服務全球患者的潛力。我們期待這一中國方案能盡快落地臨床,為結腸癌治療領域帶來變革,惠及更多患者。
論文鏈接:
https://www.cell.com/cancer-cell/fulltext/S1535-6108(25)00396-4