
中大新聞網訊(通訊員王金凱、曹楠)近日,中山大學中山醫學院王金凱教授和曹楠教授課題組合作在Nature Communications期刊發表題為“Parallel functional assessment of m6A sites in human endodermal differentiation with base editor screens”的研究論文,開發了一種基于腺嘌呤單堿基編輯的技術大規模篩選功能性的m6A RNA修飾位點,并利用該技術系統地篩選了在人胚胎干細胞向內胚層分化的的過程中發揮關鍵作用的m6A位點。論文的通訊作者是中山大學中山醫學院的王金凱教授和曹楠教授,第一作者為王金凱教授課題組的程維晟博士和曹楠教授課題組的劉芳博士。此外,王金凱教授課題組的任志軍博士在數據分析中做出了重要貢獻。
m6A(N6-methyladenosine)RNA修飾是發生在RNA腺嘌呤上含量豐富的可逆的動態修飾。王金凱教授在美國博士后期間的工作發現m6A在胚胎干細胞命運決定中發揮關鍵的作用,缺失m6A的胚胎干細胞會導致干性基因不能正常降解從而喪失分化潛能。然而由于目前并沒有方法能夠對m6A位點進行轉錄組范圍的功能篩選,因此難以系統揭示具體哪些m6A位點在胚胎干細胞細胞命運決定中發揮關鍵的作用。腺嘌呤單堿基編輯器可以直接在DNA上修改m6A修飾位點的腺嘌呤堿基,從而導致相應RNA上m6A修飾被破壞。基于這一策略,研究團隊設計了由7999條sgRNA組成的文庫,這些sgRNA可以靶向6048個不同的m6A 位點所對應的DNA。為了篩選在胚胎干細胞向內胚層分化中發揮作用的m6A位點(sgRNAs),研究團隊在人胚胎干細胞(hESCs)中通過慢病毒轉入sgRNA文庫后,誘導hESCs向內胚層分化,以CXCR4為標記通過流式細胞分選強陽性(內胚層)和陰性(非內胚層)的細胞,通過比較不同sgRNA在兩群細胞中的富集程度從而篩選出78條在非內胚層中富集的sgRNA和137條在內胚層細胞中富集的sgRNA。研究團隊選擇了分別位于SOX2和SDHAF1基因的兩個促進分化的m6A位點和一個位于ADM基因的抑制分化的m6A位點進行了功能驗證,發現這三個m6A確實是通過m6A的機制影響胚胎干細胞向內胚層分化。
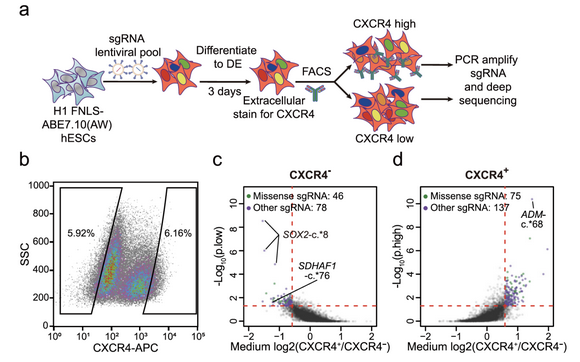
圖:m6A功能篩選的策略和篩選結果
m6A在RNA上分布廣泛,在各種病理和生理過程中都發揮了重要作用。本研究首次實現在轉錄組水平系統篩選具有特定功能的m6A位點,對理解m6A調控生命過程的具體機理和疾病靶點研究具有重要意義,也對干細胞命運調控的機理提供了新的視角。這一研究策略也有望被廣泛應用于其他領域中m6A功能位點的發掘和研究。
該工作得到了國家重點研發計劃、國家自然科學基金和廣東省自然科學基金的支持。