
中大新聞網(wǎng)訊(通訊員寇曉星)2021年9月,中山大學(xué)附屬口腔醫(yī)院寇曉星研究員團(tuán)隊(duì)在ACS Nano (影響因子15.9)發(fā)表了題為“Apoptotic Extracellular Vesicles Ameliorate Multiple Myeloma by Restoring Fas-Mediated Apoptosis”的研究論文,在凋亡囊泡(apoptotic extracellular vesicle,apoEV)生物治療領(lǐng)域取得了新的突破。細(xì)胞凋亡是維持機(jī)體內(nèi)穩(wěn)態(tài)的關(guān)鍵,并會(huì)產(chǎn)生大量凋亡囊泡。細(xì)胞凋亡的異常與自身免疫性疾病,神經(jīng)系統(tǒng)疾病,腫瘤等的發(fā)生密切相關(guān)。以往研究認(rèn)為機(jī)體產(chǎn)生的凋亡囊泡被吞噬細(xì)胞攝入、降解。 2018年,該團(tuán)隊(duì)首次在Cell Research (DOI:10.1038/s41422-018-0070-2)雜志發(fā)表研究論文,闡明凋亡囊泡可以維持體內(nèi)間充質(zhì)干細(xì)胞(Mesenchymal stem cell, MSC)及骨組織穩(wěn)態(tài);并首次以骨質(zhì)疏松為例提出干細(xì)胞來源凋亡囊泡作為新的生物治療手段用于治療疾病。
多發(fā)性骨髓瘤 (Multiple myeloma, MM) 是第二常見的血液系統(tǒng)惡性腫瘤,會(huì)導(dǎo)致包括溶骨性病變、骨痛、貧血、腎功能障礙等多種臨床癥狀,通常被認(rèn)為是一種無法治愈的疾病。包括多發(fā)性骨髓瘤在內(nèi)的許多腫瘤細(xì)胞膜表面的凋亡受體Fas的表達(dá)會(huì)減少,F(xiàn)as介導(dǎo)的細(xì)胞凋亡處于失活狀態(tài),使得腫瘤細(xì)胞能夠逃逸FasL/Fas通路介導(dǎo)的細(xì)胞凋亡。
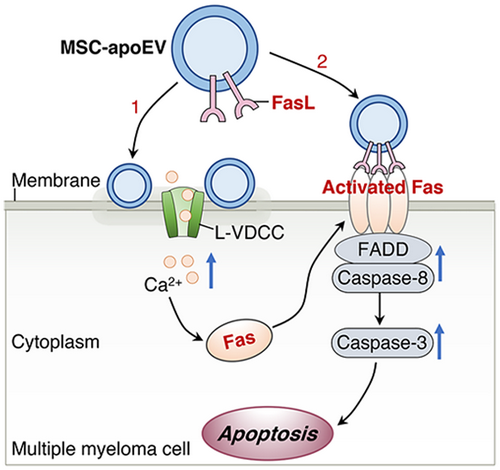
凋亡囊泡通過 “一石二鳥”的策略治療多發(fā)性骨髓瘤模式圖
該研究發(fā)現(xiàn),MSC凋亡過程中產(chǎn)生的凋亡囊泡表面高表達(dá)細(xì)胞死亡相關(guān)信號(hào)如FasL等。并發(fā)現(xiàn):(1) 全身輸注MSC來源凋亡囊泡可顯著延長(zhǎng)多發(fā)性骨髓瘤小鼠的壽命,挽救溶骨性病變,改善腎損傷;(2)凋亡囊泡在體內(nèi)外均可誘導(dǎo)多發(fā)性骨髓瘤細(xì)胞凋亡,抑制腫瘤細(xì)胞生長(zhǎng);(3)凋亡囊泡直接接觸腫瘤細(xì)胞,通過誘發(fā)Ca2+??內(nèi)流促進(jìn)Fas從細(xì)胞質(zhì)轉(zhuǎn)運(yùn)到細(xì)胞膜表面;(4)凋亡囊泡利用其膜表達(dá)的FasL激活腫瘤細(xì)胞中恢復(fù)正常的Fas通路以啟動(dòng)細(xì)胞凋亡。研究揭示了凋亡囊泡在誘導(dǎo)腫瘤細(xì)胞凋亡中的作用,并提出凋亡囊泡以一種“一石二鳥”的策略治療多發(fā)性骨髓瘤的新方法。這一發(fā)現(xiàn)為理解細(xì)胞外囊泡與腫瘤相互作用增加了新的認(rèn)識(shí),也為修飾凋亡囊泡、開發(fā)新的腫瘤治療方法開辟了道路。
這項(xiàng)工作得到了廣東高層次醫(yī)院建設(shè)計(jì)劃,珠江人才計(jì)劃,中山大學(xué)青年教師重點(diǎn)培育計(jì)劃等多個(gè)項(xiàng)目的支持。